Gentechnologie, Genmanipulation, Biotechnologie Eine einführende Übersicht (Bearbeitungsstand: )Dr. rer. nat. Rainer Bäuerlein, 59557 Lippstadt Die in diesem Artikel aufgeführten Bilder sind auch alle in einer gemeinsamen Übersicht in der Bilderdatei zu finden. Durch Anklicken können sie vergrößert werden.Inhaltsverzeichnis 1.
Biotechnologie ohne Veränderung der Gene Leider ist es in heutiger
(speziell deutscher?) Zeit üblich geworden, dass jeder zu jedem und allem alles
"weiß" und sagen kann; es ist üblich, alles zu "hinterfragen".
Wohlgemerkt, es geht nicht darum, dass Entscheidungen nicht von jedem Betroffenen genau
abgewogen werden sollen und dass etwa nur Jasager gefragt sind, sondern es geht darum,
dass dieses "Hinterfragen" zum Prinzip erhoben und über viele Instanzen bis zur
Farce fortgesetzt wird und letztlich Entscheidungen entweder verzögert oder gar
unmöglich macht. Es werden immer nur die möglichen Nachteile für die jeweilige
persönliche Situation gesehen, es scheint die langfristige Perspektive und das
Verantwortungsbewusstsein für das Ganze und die Allgemeinheit zu fehlen. Zudem fehlt in
vielen Fällen das notwendige Hintergrundwissen, das für eine sachkundige Abwägung
erforderlich ist. Dem soll diese Abhandlung ein wenig abhelfen. Die Erstere ist lange bekannt und wurde wahrscheinlich schon vor etwa
10.000 Jahren praktiziert. Zu der Zeit dürfte die erste noch ungeordnete Domestizierung
der heutigen Haushunde begonnen haben. Auch fallen in diese Zeit schon die ersten
"Zuchtversuche" mit Gräsern, sicherlich nicht von den damals lebenden Menschen
veranlasst, sondern von der Natur bewirkt, vom Menschen erkannt und genutzt. Die Auslese
wurde dann im Laufe der Zeit immer besser, weil der Mensch die Gesetzmäßigkeiten zu
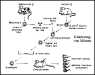
begreifen begann und sie sinnvoll nutzte. Unter Klonieren versteht man die Erzeugung genetisch identischer Organismen. 1.1.1. Zwei- bis achtzellige Keime werden in ihre Einzelzellen zerlegt. Die Zellen nehmen ihre Teilungstätigkeit wieder auf und werden in der Regel zu vollständigen Lebewesen. Ein ähnlicher Vorgang kommt in der Natur häufig vor. (Z. B. eineiige Zwillinge bei Mensch und Tier). Das Verfahren wird seit 1981 bei der Rinder- und Schafzucht (siehe Abbildungen unten links) zur künstlichen Herstellung von Mehrlingen angewandt. Man kann es auch beim Menschen anwenden, was ja, wie erst kürzlich bekannt wurde, inzwischen geschehen ist. Erste erfolgreiche Versuche machte Hans Spemann 1930 mit Schnürversuchen an Molchembryos.
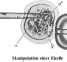 wird mit einer Mikropipette in eine Eizelle
gegeben, nachdem zuvor der weibliche Kern entfernt wurde, die damit
zu einer Zygote (befruchteten Eizelle) wird, sich teilt und zu einem neuen
Lebewesen heranwächst. Mit Fröschen wurde dies erstmals 1952 gemacht, es entwickelten sich aber nur Kaulquappen, keine
Frösche. 1962 hatte der Brite John Gurdon dann mit Fröschen Erfolg. 1981 (Karl Illmensee, Schweiz) gelang es angeblich nach eigener - nicht
nachgewiesener - Aussage erstmals mit Säugern (Mäusen). Diese Versuche sollen aber
gefälscht worden sein. Mit Menschen ist dies zurzeit noch nicht möglich (nicht
bekannt!?). Die Nachkommen sind also untereinander gleich. Die Schwierigkeit liegt hier u.a. in der Kleinheit der Säugereizellen (z. B. 0,2 mm beim Menschen). 1983 hat Davor
Solter vom Max-Planck-Institut für Immunbiologie in Freiburg durch Elektrofusion Schafe
geklont. wird mit einer Mikropipette in eine Eizelle
gegeben, nachdem zuvor der weibliche Kern entfernt wurde, die damit
zu einer Zygote (befruchteten Eizelle) wird, sich teilt und zu einem neuen
Lebewesen heranwächst. Mit Fröschen wurde dies erstmals 1952 gemacht, es entwickelten sich aber nur Kaulquappen, keine
Frösche. 1962 hatte der Brite John Gurdon dann mit Fröschen Erfolg. 1981 (Karl Illmensee, Schweiz) gelang es angeblich nach eigener - nicht
nachgewiesener - Aussage erstmals mit Säugern (Mäusen). Diese Versuche sollen aber
gefälscht worden sein. Mit Menschen ist dies zurzeit noch nicht möglich (nicht
bekannt!?). Die Nachkommen sind also untereinander gleich. Die Schwierigkeit liegt hier u.a. in der Kleinheit der Säugereizellen (z. B. 0,2 mm beim Menschen). 1983 hat Davor
Solter vom Max-Planck-Institut für Immunbiologie in Freiburg durch Elektrofusion Schafe
geklont. Im Februar 1997 wurde "Dolly" geboren (gestorben Februar 2003), ein Schaf, das auf diese Weise in Schottland gezeugt wurde. "Dolly" ist genetisch völlig identisch mit dem Schaf, das den Kern einer Euterzelle lieferte, hat aber auch Plasmagene des Schafes, das die entkernte Eizelle lieferte. Es wurde von einer Leihmutter ausgetragen, die mit den beiden vorherigen nicht identisch ist. Somit hat "Dolly" drei "Mütter". Laut Ian Wilmut vom Roslin-Institut in Edinburgh haben geklonte Tiere eine höhere Sterblichkeit und werden größer. Die Gründe dafür sind nicht bekannt. Die Erfolgsquote lag Ende 1998 bei 1,3 - 1,4%. 2001 hat Ian Wilmut sich in "Science" (Band 291, S. 2552) zu Wort gemeldet und vor der Klonung von Menschen gewarnt. Die meisten Klone stürben noch als Embryos. Die Überlebenden erlägen dann aber meist Atem- und Kreislaufbeschwerden. Ferner gäbe es gehäuft Nierenversagen, Störungen des Immunsystems, abnorme Hirnfunktionen und gehäufte Organmissbildungen. Bei Menschen sei mit den gleichen Erscheinungen zu rechnen. Er möchte seine Warnungen jedoch nicht auf das Klonen von menschlichen Stammzellen bezogen sehen. Dieses Klonen halte er für sehr sinnvoll. "Dolly" war genetisch so alt wie das Tier, von dem der Kern stammt. Sie alterte also schneller und war eigentlich schon ein Greis und wog bei ihrer Geburt mehr als herkömmliche Schafe. Außerdem litt sie an typischen Alterserkrankungen (z.B. Arthritis). Man vermutet die Ursache in den Telomeren, die sich bei älteren Zellen von Teilung zu Teilung, verkürzen und letztendlich so die Zellen (DNA) altern lassen (Hayflick-Limit, benannt nach Dr. Leonhard Hayflick, der die Telomere in den 60er Jahren entdeckte). Das inzwischen bekannte Telomerase-Gen könnte eingebaut werden und sorgt dann für den Erhalt der Telomeren. Das wiederum könnte das Wuchern von Krebszellen fördern oder gar ermöglichen (sofern die Ursache nicht in gehäuften Radikalen liegt). Wenig später wurde bekannt, dass bereits im Dezember 1996 in Neuseeland Ähnliches geglückt ist. Im Juni 1997 hat das gleiche Institut "Polly" (aus embryonalen Zellen) gezüchtet, ein Schaf, dem zusätzlich ein menschliches Gen eingepflanzt wurde, das menschliche Eiweiße mit der Milch produziert (siehe dazu auch Transgene in 2.2.). Am 23. 12.98 wurde "Uschi" geboren, ein geklontes Kalb der Universität München. Im August 1996 soll in den USA ein Rhesusaffenpärchen geklont worden sein. Bei der ICSI-Methode (siehe 1.3.2.1.) soll es zu (zufälligen) Klonungen gekommen sein. Anfang Januar 1998 machte der Amerikaner Richard Seed Schlagzeilen, weil er ankündigte, ein Institut zur Klonung von Menschen gründen zu wollen. Dies ist in Deutschland nicht möglich, weil das Embryonenschutzgesetz dies verbietet. Im Januar 1998 wurde in den USA ein Kalb nach der "Dolly-Methode" aus embryonalen Zellen geklont und war ebenfalls Träger von Transgenen (siehe auch 2.2.). Am 5. März 2000 wurden nach der "Dolly"-Methode in den USA transgene Schweine geklont. (Siehe auch 2.2.4.) Japaner sollen laut dpa im Sommer 1998 embryonale Zellen aus der Milch von Kühen für Klonversuche angewendet haben. Diese Methode würde Körpereingriffe unnötig machen. Anfang 2000 wurden in den USA Rinder geklont und so Sechslinge gezeugt, die genetisch jünger sind als normale Jungtiere. Sie sollen aus Stammzellen gezeugt worden sein und sollen deutlich länger leben können. Ende Dezember 2002 soll "Eve", ein Mädchen, in den USA als erstes menschliches Klonkind geboren worden sein, das verkündigte die französische Wissenschaftlerin Brigitte Boisselier (Firma Clonaid), Mitglied der Sekte der Raelianer. Dieselbe Forscherin verkündete, in den ersten Januartagen 2003 sei das zweite Klonkind in Holland geboren worden, ein drittes würde bald 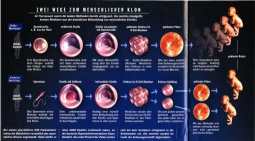 folgen. Beweise dafür wurden jedoch nicht erbracht. Der italienische Arzt Severino Antinori hat für Januar 2003 ebenfalls die Geburt eines Klonbabies angekündigt.
Bis Mai 2006 hat man nichts mehr von diesen Ankündigungen gehört. folgen. Beweise dafür wurden jedoch nicht erbracht. Der italienische Arzt Severino Antinori hat für Januar 2003 ebenfalls die Geburt eines Klonbabies angekündigt.
Bis Mai 2006 hat man nichts mehr von diesen Ankündigungen gehört.Wurden für die Zeugung von "Dolly" 291 Embryonen "verbraucht", so rechnet man beim Menschen mit einem etwa fünfmal so hohen Wert. Wege der menschlichen Klonung soll die linke Graphik aus FOCUS 49/2002 zeigen. Klonschweine haben vergrößerte Organe. Auch bei Kühen hat man, wie bei Dolly, erhöhte Geburtsgewichte festgestellt. Ursache dafür könnte das bei geklonten Tieren häufig fehlerhaft arbeitende Steuerung des Wachstumsgens IGF2R sein. Auch bei Affen und Mäusen tauchten gravierende Schäden auf (~95%). Keith Killian vom Duke University Medical Center in Durham (North Carolina) hat festgestellt, dass beim Menschen das Wachstumsgen nicht dieser Steuerung unterliegt und somit eine Chance besteht, hier schneller voran zu kommen als vermutet (wenn dies denn erwünscht sein sollte). 1.1.3. Forscher der US-Firma Advanced Cell Technology (ACT) in Worcester (Massachusetts) verschmolzen die entkernte Eizelle einer Kuh mit dem Zellkern einer menschlichen Zelle. Man hofft nun, diese Hybridzellen weiter züchten zu können, um daraus menschliches Gewebe für den Menschen gewinnen zu können, von dem die Zelle stammt. Dieses Gewebe würde nicht abgestoßen. Im Juni 1999 teilte ACT mit, dass es ihnen gelungen sei, aus mit Kernen von menschlichen Hautzellen versehenen entkernten Kuheizellen menschliches Gewebe zu züchten. Es seien frühe menschliche Embryonen mit etwa 400 Zellen entstanden. Die amerikanische Firma Geron forscht in der gleichen Richtung. (laut FOCUS 25/99) 1.1.4. Pflanzengewebe wird vorsichtig zerteilt und auf speziellen Nährböden (z.B. Agar-Agar) weiter zur natürlichen Teilung gebracht. Die spezialisierten Zellen werden wieder totipotent und langsam wächst aus dem Zellhaufen unter einem Wundverschluss (Kallus) ein kleines neues vollständiges Pflänzchen hervor, das später dann ausgepflanzt werden kann und zur vollen Größe heranwächst. 1.1.5. Im Mai 2005 wurde bekannt, dass südkoreanische Forscher aus Körperzellen von Patienten embryonale Stammzellen hergestellt haben. Dazu wurden Hautzellen in entkernte Eizellen implantiert. Pro Patient benötigten die Forscher 17. Eizellen. Es wurden 242 Eizellen gebraucht, um eine Zelllinie herzustellen. Die geklonten Eizellen wurden in einer speziellen Nährlösung zur Teilung veranlasst. Die Ergebnisse wurden inzwischen als Fälschung entlarvt. 1.1.6. Belinda Chang von der University of Toronto baut aus Fossilien Gene ausgestorbener Tiere nach. In fossilen Knochen kann noch genetisches Material gefunden werden, aber ob je ein ganzes Genom gefunden werden kann, ist arg zu bezweifeln. 1.1.7. 2007 wurden in Seoul 6 an der Universität geklonte Labrador Retriever eines Drogenspürhundes geboren, die 2009 als Drogenspürhunde eingesetzt wurden. Damit will man genetische Fähigkeiten der Hunde nutzen, da die Suche nach geeigneten Hunden schwierig ist.
1.2.1.
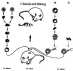
1.2.2. Man injiziert embryonale Zellen eines Tieres in den Keim eines anderen (Injektionschimäre = obere linke Abbildung b + c). Dies wurde 1980 erstmals mit Mäusen durchgeführt. 1.2.3. Auch die Lebewesen, die aus der Verschmelzung von Keimzellen naher verwandter Tiere hervorgehen, nennt man Chimären. So sind Maultier und Maulesel entstanden. Diese Lebewesen sind jedoch unfruchtbar. Eine solche Chimäre ist auch die "Tomoffel", eine Verschmelzung von Protoplasten der Kartoffel und der Tomate. Die Pflanze oberhalb der Erde produziert Tomaten, unter der Erde Kartoffeln. 1.2.4. Anfang April 2008 verlautete aus dem Institut für Humangenetik der Universität Newcastle in England, dass dort Stammzellen aus Eizellen einer Kuh und genetischem Material des Menschen geschaffen worden sind. Nach Auskunft des Direktors des Institute, Lyle Armstrong, wurde lediglich 0,1 % tierischen Materials benutzt.Da es sowohl praktisch als auch ethisch schwierig ist, an menschliche Eizellen zu kommen, sei dieser Weg beschritten worden, um zu erforschen, ob die so gewonnen Zellen geeignet sind, daran Stammzellenforschung zur Behebung menschlicher Krankheiten durchzuführen. Die so erzeugten Chimären wurden nach drei Tagen abgetötet. Gesetzlich möglich sind 14 Tage, was auch ausprobiert werden soll. Ähnliche Forschungen sind aber schon aus den Kings-College in London bekannt. Ebenso von der amerikanischen Biotech Firma ACT, wo menschliche Hautzellen mit Eizellen von Kühen verschmolzen wurden. Ferner sind ähnliche Versuche bekannt aus Südkorea (2002) und China (2003), letztere wurden und in "Cell Research" veröffentlicht.
 die Gebärmutter (in vivo). 1997 wurden in Deutschland etwa 14% aller Schwangerschaften
als in vitro-Schwangerschaften erzeugt. (Etwa 1,5 Millionen Paare in Deutschland sind
ungewollt kinderlos). Man spricht hier auch von Embryotransfer (siehe Abbildung links)
oder von den Retortenbabys, besonders dann, wenn man an menschliche Nachkommen denkt. Die
so gewonnenen Embryonen können jeder beliebigen Frau implantiert oder aber einer
Genmanipulation zugeführt oder für spätere Zeiten aufgehoben werden, indem man sie
einfriert (Kryokonservierung, kryos = Frost). Als erstes Retortenbaby wurde Louise Brown
bekannt (s. Photo
unten), die am 25. Juli 1978 in England geboren wurde.
"Vater" war Prof. Robert Edwards, der 2010 dafür den Nobelpreis für
Medizin erhielt. Ende 2006 bekam sie
ihr eigenes Kind Cameron.
Man spricht hier auch von einer extrakorporalen Befruchtung, da sie außerhalb des Körpers stattfindet. Diese Art der
Zeugung setzt eine gewisse Technik und Vorausschau voraus. So werden häufig mehrere
Embryonen gezeugt und implantiert, um dieses aufwändige und belastende Verfahren nicht
unnötig oft wiederholen zu müssen. Es werden also "Ersatzembryonen"
vorgehalten. Die Chancen für eine Schwangerschaft bei einem Embryotranfer betragen etwa
10 bis 15%, bei drei implantierten Embryonen etwa 15 bis 30%. Ungefähr 90% der in vitro
befruchteten Eier kommen zur Teilung bis zum Vier-Zellstadium. Circa 60 Stunden nach der
Insemination (Besamung) wird im Acht-Zellstadium reimplantiert. Überschüssige Embryonen
werden für Versuchszwecke im Labor verwendet oder mit der Kryotechnik für später
konserviert. Durch Teilung von Embryonen kann man, so makaber es auch klingen mag, ein
"Ersatzteillager" anlegen. Am 16. April 1982 wurde Oliver als
erstes deutsches Retortenbaby im Universitätsklinikum Erlangen geboren. die Gebärmutter (in vivo). 1997 wurden in Deutschland etwa 14% aller Schwangerschaften
als in vitro-Schwangerschaften erzeugt. (Etwa 1,5 Millionen Paare in Deutschland sind
ungewollt kinderlos). Man spricht hier auch von Embryotransfer (siehe Abbildung links)
oder von den Retortenbabys, besonders dann, wenn man an menschliche Nachkommen denkt. Die
so gewonnenen Embryonen können jeder beliebigen Frau implantiert oder aber einer
Genmanipulation zugeführt oder für spätere Zeiten aufgehoben werden, indem man sie
einfriert (Kryokonservierung, kryos = Frost). Als erstes Retortenbaby wurde Louise Brown
bekannt (s. Photo
unten), die am 25. Juli 1978 in England geboren wurde.
"Vater" war Prof. Robert Edwards, der 2010 dafür den Nobelpreis für
Medizin erhielt. Ende 2006 bekam sie
ihr eigenes Kind Cameron.
Man spricht hier auch von einer extrakorporalen Befruchtung, da sie außerhalb des Körpers stattfindet. Diese Art der
Zeugung setzt eine gewisse Technik und Vorausschau voraus. So werden häufig mehrere
Embryonen gezeugt und implantiert, um dieses aufwändige und belastende Verfahren nicht
unnötig oft wiederholen zu müssen. Es werden also "Ersatzembryonen"
vorgehalten. Die Chancen für eine Schwangerschaft bei einem Embryotranfer betragen etwa
10 bis 15%, bei drei implantierten Embryonen etwa 15 bis 30%. Ungefähr 90% der in vitro
befruchteten Eier kommen zur Teilung bis zum Vier-Zellstadium. Circa 60 Stunden nach der
Insemination (Besamung) wird im Acht-Zellstadium reimplantiert. Überschüssige Embryonen
werden für Versuchszwecke im Labor verwendet oder mit der Kryotechnik für später
konserviert. Durch Teilung von Embryonen kann man, so makaber es auch klingen mag, ein
"Ersatzteillager" anlegen. Am 16. April 1982 wurde Oliver als
erstes deutsches Retortenbaby im Universitätsklinikum Erlangen geboren.
Einige Zahlen: 54% aller bisherigen (2010) registrierten künstlichen Befruchtungen fanden in Europa statt. 3 von hundert Kindern in Skandinavien sind Retortenkinder, in Deutschland, England und Frankreich 1 - 2. 2008 wurden in Deutschland 68.000 (davon 11.000 in NRW) Versuche bei 44.000 Frauen durchgeführt. Etwa ein Drittel war erfolgreich. Eine Behandlung kostet im Schnitt etwa 3.600 €. Im Oktober 2008 wurde in Spanien der Sohn Javier von Andres und Soledad Marical in Sevilla geboren. Er ist ein so genanntes "Designer-Baby", ein Retortenbaby, das nach einer Präimplantationsdiagnostik unter mehreren Embryonen ausgesucht wurde, damit es seinem 6 Jahre älteren Bruder Andres, der an Thalassämia major leidet, als Stammzellenspender zur Verfügung stehen kann. Laut Bericht der englischen Zeitung "Independent on Sunday" vom Oktober 1998 wollen englische Forscher jedem Kind einen "genetischen Zwilling" zur Seite stellen, der im Falle einer notwendigen Gewebeübertragung als Zelllieferant zur Verfügung steht. In der Zeitschrift "Science" vom Oktober 1998 stellt der Amerikaner James Thompson von der Universität Wisconsin ein Verfahren zur Gewinnung embryonaler Stammzellen vor, die später als Ersatz von Organen dienen sollen. Während normale Schwangerschaften in 30 bis 60% erfolgreich sind, sind dies bei der in-vitro-Fertilisation in der Regel nur etwa 10 bis 20%. 1982 wurde in Deutschland das erste Kind in vitro gezeugt. Bis März 2008 wurden weltweit etwa 3.500.000 IVF-Kinder geboren. In Deutschland werden etwa 1,2 % aller Kinder als IVF-Kinder geboren. Die Erfolgsquote bei der künstlichen Befruchtung liegt zwischen 20 und 30%. Nach Untersuchungen, die die australischen Krankenkassen im Frühjahr 2012 in Auftrag gegeben hatten (Veröffentlicht in "New England Journal of Medicine") gibt es bei der IVF gegenüber normalen Schwangerschaften kein höheres Gesundheitsrisiko für die Kinder In-vitro-Maturation (IVM). An der Universität Lübeck wurde eine Methode entwickelt, um krebserkrankten Frauen eine spätere Empfängnis zu ermöglichen. Vor der Bestrahlung bzw. Chemotherapie werden unreife Eizellen entnommen und tiefgefroren. Die Reifung erfolgt dann später. Es wurden bereits Kinder so gezeugt . Inzwischen gehen Bestrebungen dahin, die IVF durch die IVM zu ersetzen, weil die intensive, belastende und zeitaufwändige Behandlung der Frauen unterbleiben kann. Es werden unreife Eier entnommen und in Nährlösung in wenigen Tagen zur Reifung gebracht. Im Oktober 2007 wurden in England so gezeugte Zwillinge geboren1.3.1. Mann und Frau können normal keine Kinder zeugen, weil z.B. die Eileiter unpassierbar sind, ihre Keimzellen sind aber voll funktionsfähig. Die Zeugung erfolgt in vitro mit anschließender Reimplantation. 1.3.2. Der Mann ist unfruchtbar (dies macht etwa 35% der Fälle ungewollter Kinderlosigkeit aus). Ursache dafür können unbewegliche oder gänzlich unfruchtbare Spermien sein. 1.3.2.1. Eine Art zur Zeugung ist hier die ICSI
(Intracytoplasmatische Spermieninjektion). Hierbei werden die unbeweglichen Spermien
direkt den Hoden entnommen und in eine Eizelle injiziert. Die Schwangerschaftsrate hierbei
beträgt etwa 30%. ICSI ist teilweise umstritten, weil bei einer Untersuchung in den
Niederlanden 1997 festgestellt wurde, dass 26% dieser Männer genetische Schäden haben
(u.a. Muskoviszidose). Weltweit wurden bis März 2000 etwa 100.000 Kinder gezeugt, davon
in Deutschland etwa 30.000. Die aktuellen Zahlen für Deutschland im
Jahr 2007 sind 6.000 Kinder. Im Krankenhaus Berlin-Westend wurden
1.000 ICSI-Eizellen produziert, wovon 300 zum Erfolg führten. Untersuchungen in Australien aufgrund eines Forschungsauftrages der gesetzlichen Krankenkassen ergab, dass 10% der so gezeugten Kinder mit Beeinträchtigungen zur Welt kommen. (New England Journal of Medicine). 1.3.2.2. Ein fremder, (der Frau) unbekannter Mann ist Spermaspender (meist aus der Kryobank). 1.3.3. Die Frau ist unfruchtbar. Befruchtung in vitro mit anschließendem Reimplantat. 1.3.4. Mann und Frau sind unfruchtbar. Das von der Mutter ausgetragene Kind ist mit seinen Eltern nicht verwandt. 1.3.5. Die Frau ist fruchtbar, trägt aber in diesem Fall ein fremdes Kind für eine nicht gebärfähige Frau aus. Hier haben wir es mit dem umstrittenen Problem der "Leihmutter" zu tun. Bereits 1890 wurde dieses Prinzip erstmals bei Kaninchen erfolgreich eingesetzt. Erst 1956 gelang es dann, ein Kulturmedium herzustellen, in dem Tierembryonen gezüchtet werden konnten, und 1959 konnten erstmals menschliche Zellen in einer Nährlösung herangezogen werden. Es wurden auch menschliche Embryonen in einer künstlichen Gebärmutter herangezogen."Leihmütter" sind in Deutschland verboten. Jährlich werden etwa 3,7 Millionen Retortenbabys geboren (Stand Frühjahr 2012). 1.4. Eingriff in die Embryonalentwicklung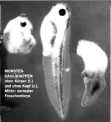 Der englische Embryologe
Professor Slak züchtete Kaulquappen des Krallenfrosches Xenopus, die er mit dem
Fibrioblasten-Wachstumsfaktor (FWF) behandelt. Damit kann man u. a. ein Gen namens
"Hox" beeinflussen, das die Ausbildung von Schwanz und Kopf steuert. Durch
gezielte Überhöhung der FWF-Konzentration kann man Embryonen ohne Schwanz oder ohne Kopf
oder nur mit Kopf züchten (siehe linke Abbildung).
Ziel dieser Forschung soll es
sein, Tiere (Menschen) ohne Zentralnervensystem (ZNS) zu züchten, die als Ersatzteillager
fungieren können. Letztendlich könnten dann auch nur einzelne Organsysteme oder
Körperteile gezüchtet werden. Die Überlegung dabei ist, dass ja ein Lebewesen (ein
Mensch) kein Lebewesen (kein Mensch) ist, wenn er kein ZNS hat. Der englische Embryologe
Professor Slak züchtete Kaulquappen des Krallenfrosches Xenopus, die er mit dem
Fibrioblasten-Wachstumsfaktor (FWF) behandelt. Damit kann man u. a. ein Gen namens
"Hox" beeinflussen, das die Ausbildung von Schwanz und Kopf steuert. Durch
gezielte Überhöhung der FWF-Konzentration kann man Embryonen ohne Schwanz oder ohne Kopf
oder nur mit Kopf züchten (siehe linke Abbildung).
Ziel dieser Forschung soll es
sein, Tiere (Menschen) ohne Zentralnervensystem (ZNS) zu züchten, die als Ersatzteillager
fungieren können. Letztendlich könnten dann auch nur einzelne Organsysteme oder
Körperteile gezüchtet werden. Die Überlegung dabei ist, dass ja ein Lebewesen (ein
Mensch) kein Lebewesen (kein Mensch) ist, wenn er kein ZNS hat. Alternativ dazu könnte dies auch bei einer deutlichen Verbesserung der Klonierungstechnik erreicht werden, d. h., es können Organkulturen angelegt werden.
|
||||
1.5. Eingriff in den Zeugungsakt US-Wissenschaftler am Institut
für Genetik in Fairfax haben eine Methode entwickelt, die es mit sehr großer Sicherheit
erlaubt, das Geschlecht des zukünftigen Kindes zu bestimmen. Es wird dabei der
Unterschied der X- und Y-Chromosomen in den Spermien genutzt. Die Y-Chromosomen haben eine
andere DNA und zudem ~2,8% weniger. Die DNA wird mit fluoreszierenden Farben behandelt und
so nachgewiesen.
Im Blickpunkt der Diskussion steht heute verstärkt die Forschung an Stammzellen. Der Deutsche Bundestag hat begrenzte gesetzliche Grundlagen für die deutsche Forschung beschlossen. So dürfen nur Stammzellen benutzt werden, die von vor dem 1. Mai 2007 stammen. Die beiden folgenden Artikel vom 30. Januar 2002 des Berliner Tagesspiegel sollen hier stellvertretend als erste Information abgedruckt werden. 1.6.1. Die Debatte um den Import und die Erforschung embryonaler Stammzellen ist mit Fachausdrücken durchsetzt. Im folgenden werden Begriffe, die bei der Bundestagsdebatte zur Bioethik immer wieder fallen, erläutert. Die Grundlagen Ein Embryo entsteht
bei der Befruchtung (Konzeption). Das ist die Verschmelzung von Ei- und Samenzelle. Die
Chromosomen beider Zellen vereinigen sich damit zu einem neuen, individuellen Genom. Dies
kann in vivo, im Körper der Frau, oder in vitro,
wörtlich: im Reagenzglas, also im Labor bei einer invitro-Fertilisation (IVF), geschehen. Das Kernthema Der menschliche Körper
besteht aus verschiedenen spezialisierten Zelltypen, die unterschiedliche Aufgaben
übernehmen. Zu Beginn jedoch bestehen wir aus einer Zelle: Der befruchteten Eizelle. Sie
ist gewissermaßen die erste Stammzelle. Aus ihr können - und müssen -
alle anderen Arten von Zellen entstehen. Mediziner nennen sie deshalb totipotent,
wörtlich "allmächtig". Diese universelle Fähigkeit verliert sich nach Ansicht
der Entwicklungsbiologen spätestens im Acht-Zell-Stadium. Bis dahin könnte aus jeder
Zelle des frühen Embryos theoretisch aber noch ein ganzer Mensch werden. Mit dem Begriff
Stammzelle wird aber allgemeiner jede noch nicht ausdifferenzierte Zelle bezeichnet, die
sich teilen und entwickeln kann. Stammzellen können von einem Embryo, einem Feten, einem
Kind oder einem Erwachsenen stammen. Die Ziele Mit adulten und embryonalen Stammzellen verbinden sich große Hoffnungen auf Therapien durch Gewebeersatz. Von der Forschung mit menschlichen embryonalen Stammzellen erhoffen sich die Forscher außerdem auch Aufschluss über die molekularen Grundlagen der Entwicklung des frühen Embryos. Dieses Verständnis könnte die Voraussetzung dafür sein, dass es gelingt, umgekehrt auch die Reprogrammierung adulter Stammzellen zu bewerkstelligen. Ein solches Zurückspulen der Spezialisierung könnte die ethisch unbedenklichen adulten Stammzellen universeller einsatzbereit machen. (ADELHEID MÜLLER-LISSNER) 1.6.2. Tricks abgucken und patentieren. (pet) Wolfgang Rüdinger hat unruhige Stunden vor sich. Für den Chef des Biotech-Start-ups Cytonet hängt viel von dem heutigen Votum des Bundestages ab: Entscheiden sich die Parlamentarier gegen den Import embryonaler Stammzellen, wird er wohl einen Teil der Produktion ins Ausland verlagern. Rüdinger: "Wenn die Entscheidung gegen den Import von embryonalen Stammzellen ausfällt, ist das ein klarer Wettbewerbsnachteil für den Standort Deutschland." Cytonet mit Sitz im nordbadischen Weinheim ist eines der wenigen deutschen Biotech-Unternehmen, die sich mit der Stammzelltherapie beschäftigen. Zusammen mit der Medizinischen Hochschule Hannover entwickelt es Leberzellen für Leberzelltransplantationen Cytonet-Chef Rüdinger hofft dabei auf die Hilfe der embryonalen Stammzellen. "Wir starten mit adulten Stammzellen, würden uns aber gern den einen oder anderen Trick von der embryonalen Stammzelle abgucken" sagt er. Ziel sei es, eigene Patente anzumelden - und damit Wettbewerbsrechte zu sichern. Die embryonale Stammzelle als Lehrmeister zu haben, könne das Ganze beschleunigen. Auf Import-Stammzellen mag sich der Unternehmer nicht verlassen - aus gutem Grund. Wenn embryonale Stammzellen aus dem Ausland importiert werden, dann gehören die wirtschaftlichen Rechte dem, der diese Zellen isoliert hat, sagt Rüdinger. Deutsche Wissenschaftler betrieben dann eine kostenlose Auftragsforschung für das Ausland. Er drängt daher auf eine weitergehendere Lösung: Die begrenzte Freigabe überschüssiger Embryonen auch in Deutschland. Man sollte sich durchringen, unter sehr gut kontrollierten Bedingungen auch Embryonen, die in Deutschland existent sind, in geringer Stückzahl freizugeben. Doch erstmal wartet Rüdinger das Bundestags-Votum am Nachmittag ab. 1.6.3. Daten und Anmerkungen zu den adulten Stammzellen. Im Mai 2001 wollen Forscher der Yale-University nachgewiesen haben, dass erwachsene Stammzellen doch sehr flexibel sind. So transformierten sich Mausstammzellen aus dem Knochenmark z. B. zu Gewebe des Darms, der Speiseröhre und der Lunge. Es gibt aber Hinweise darauf, dass diese Zellen zuvor mit embryonalen Stammzellen verschmolzen wurden und dann erst mit der Differenzierung begannen. Zudem hätten sie dann den doppelten normalen Chromosomensatz. Lübecker Forscher haben im Frühjahr 2004 angeblich adulte Stammzellen aus Bauchspeicheldrüsen gewonnen, die sich wie embryonale Stammzellen verhalten sollen. Erschienen ist dazu eine Veröffentlichung in der ziemlich unbekannte Zeitschrift "Applied Physicist A". Prof. Hans Schöler bezweifelt aber diese Möglichkeit. Anfang August 2006 soll es Forschern der Firma "Advanced Cell Technology" in Worchester (Massachusetts - USA) gelungen sein, Stammzellen aus Embryos zu gewinnen, ohne die Embryos zu zerstören. Die Forscher um den Wissenschaftler Robert Lanza entnahmen Embryonen im etwa Zehnzellstadum eine einzelne Zelle. Diese Technik ist eigentlich nicht neu und wird bei der Überprüfung auf Anomalien bei der IVF durchgeführt. Neu ist nur, dass es offensichtlich gelungen ist, aus einer einzelnen embryonalen Stammzelle eine Kultur zu ziehen. Anfang 2007 wurde berichtet, dass Forscher des MIT in Cambridge/Massachusetts unter Leitung von Rudolf Jaensch vier Gene mit Hilfe von Retroviren in adulte Maushautzellen übertragen haben. Dabei soll etwa eine von etwa 10.000 dieser Hautzellen in einen Embryonalzustand versetzt worden sein. Ob diese Stammzellen so gut funktionieren wie echte Embryonalstammzellen, wird von Tom Okarma von der kalifornischen Biotechnologiefirma Geron angezweifelt, zumal eines der eingeschleusten Gene als carcinogen gilt. Am 21. September 2007 veröffentlicht der Direktor der Universitätsklinik für Kardiologie in Düsseldorf, Prof. Dr. Bodo-Eckehard Strauer, in der Deutschen Medizinischen Wochenschrift Ergebnisse mit adulten Stammzellen aus dem Knochenmark. Diese wurden einem 64jährigen Patienten mit Herzinfarkt übertragen, der danach wieder genesen sei. Die Übertragung erfolgte mit einem Ballonkatheter direkt in die Infarktarterie, also mit der auch sonst üblichen Herzkathetertechnik.. Im Januar 2008 brach erneut eine Diskussion über Stammzellen aus und die Parteien des Bundestages diskutierten, ob das Arbeiten mit embryonalen Stammzellen nicht ganz verboten und der Import von ausländischen embryonalen Stammzellen nicht gänzlich untersagt werden soll. Nunmehr wurde der Stichtag für importierte Embryonen auf ein Datum vor dem 1. Mai 2007 festgelegt. Im April 2008 wurden erneut Versuche mit Stammzellgewinnung aus chimären Zellen in England bekannt, die dort gesetzlich abgesichert wurde, was zu heftigen Protesten weltweit führte (siehe unter 1.2.4). Im Juli 2008, so wird gemeldet, soll es dem Münsteraner
Professor Hans Schöler (MPI für molekulare Biomedizin, Münster) gelungen sein, aus Zellen von Mäusehoden embryonale
Stammzellen zu gewinnen. Die Technik der Gewinnung dieser Zellen,
die es erlauben würden, angepasste Zellen mit dem Erbgut des Patienten
herzustellen, ist zur Zeit noch nicht veröffentlicht. Sie stehen als gPS
den embryonalen Stammzellen näher als die des Japaners Shinya Yamanaka (iPS).
Aus Schölers Zellen sollen an der Universität Bonn bereits funktionsfähige
Muskel- und Nervenzellen gezüchtet worden sein.
Im Februar 2009 wird bekannt, dass in China 5 Klon-Embryonen hergestellt wurden. Einer der Klone stamme angeblich aus Leukozyten eines Parkinson-Patienten, an dem wegen der Erkrankung geforscht werden soll. Fernziel sei es, dieses therapeutische Klonen zur Behandlung von Krankheiten durch patienteneigene Stammzellen zu verwenden. Im April 2009 wird gemeldet, dass es einem deutsch-amerikanischem Forscherteam, u.a. Prof. Schöler vom MPI in Münster, gelungen sei, Mäusezellen nicht durch Einschleusen von Genen, sondern von Proteinen in embryonale Stammzellen zurückversetzt zu haben (piPS-Zellen). Das wäre dann der entscheidende Durchbruch. Nun geht es darum, dieses Verfahren auf menschliche Stammzellen zu übertragen. Damit wäre dann die Gefahr der Entartung oder des Ausfalls von Genen, die bei der Einschleusung von fremden Genen in die zu entwickelnde Stammzelle möglich ist, auszuschalten. Ebenfalls im Februar 2009 meldet die die Zeitschrift "Proceedings of the National Academy of Sciences", dass Bonner Forscher um Prof. Oliver Brüstle aus menschlichen embryonalen Stammzellen so genannte Gehirnstammzellen entwickelt hätten, die in Mäusegehirne eingepflanzt wurden und dort mit den Zellen kommunizierten. Die Zellen könnten unbegrenzt im Labor vermehrt werden. Im Januar 2009 lässt die Gesundheitsbehörde FDA in Bethesda (USA) erstmals Versuche der Firma Geron mit Stammzellen an 10 querschnittsgelähmten Menschen zu. Die Stammzellen sollen ins Rückenmark gespritzt werden um zu überprüfen, ob die embryonalen Stammzellen verträglich und in der Lage sind, Lähmungen zu reduzieren. Gleichzeitig soll es der Prüfung der Sicherheit der Stammzellentherapie dienen. Im Juni 2009 erscheint in der Fachzeitschrift "Stem cells and Development" eine Arbeit aus dem Labor von Karim Nayernia an der Universität Newcastle (England), in der die Herstellung von menschlichen Spermien aus Stammzellen beschrieben wird. Eine Überprüfung der Funktionsfähig der Spermien konnte noch nicht vorgenommen werden, da das nach englischem Recht verboten ist. Im August 2009 wird aus dem MPI in Münster (Prof. Schöller) gemeldet, dass es gelungen sei, durch Veränderung von nur einem Gen menschliche Nervenzellen zu iPS-Zellen "zurück zu drehen". Damit kann ein mögliches Krebsrisiko noch weiter eingedämmt werden. In Deutschland werden jährlich etwa 2000 Kinder geboren. In den meisten Fällen werden die Nabelschnüre als biologischer Müll entsorgt. Es macht stattdessen Sinn, diesen Nabelschnüren kindliches Blut zu entnehmen, das reichlich Stammzellen enthält. Z.Z. können Eltern das Blut gegen Gebühr konservieren lassen oder aber ohne Gebühr der Allgemeinheit zur Verfügung stellen. Der Rückgriff auf eigene Stammzellen komme nur in 30 Fällen auf 2,5 Millionen Spenden vor (Prof. Ursula Creutzig, Gesellschaft für pädiatrische Onkologie, Frankfurt). Ein Beispiel sei ein Kind, dass nach einem Herzstillstand eine Gehirnschädigung davontrug. Nach Behandlung mit eigenem Nabelschnurblut wanderten Stammzellen in das Gehirn ein; das Kind ist auf dem Weg der Besserung. Die dpa meldet am 31. Januar 2011: „In elf Tagen
gelangten wir von Hautzellen in einer Kulturschale zu schlagenden
Herzzellen“, sagte Studienleiter Sheng Ding vom Scripps Research Institute
in La Jolla, Kalifornien. Bislang mussten Forscher die Zellen immer erst
in ein Embryonalstadium zurücksetzen, um neue Zelltypen herzustellen. Ding
und Kollegen nahmen nun im Versuch mit Mäusezellen eine Abkürzung und
beschreiben die Technik im britischen Fachjournal „Nature Cell Biology“.
Im Mai 2013 veröffentlichte die Oregon Health & Science University in Portland ein Verfahren (unter der Leitung von Shoukhrat Mitalipov) zur Herstellung von Stammzellen aus Hautzellen. Dazu wird in eine kernlose Eizelle die DNA der Hautzelle des zukünftigen Patienten eingebracht und bis zur Blastozyste zur Teilung gebracht. Die Zellen der Blastozyste werden dann als Stammzellen weiter kultiviert, die Blastozyste selbst dabei zerstört. Ziel dabei soll es sein, in Zukunft Krankheiten wie MS, Parkinson, Herzerkrankungen oder Nervenzellen zu heilen. Der Bonner Stammzellenforscher Oliver Brüstle warnt vor zu hohen Erwartungen, andere sehen ethische Probleme, weil menschliche Embryonen geklont werden, um zu experimentieren und sie letztlich zu zerstören. In Deutschland ist ein derartiges Verfahren gesetzlich verboten. Im November 2017 wird in der "NATURE" über einen Erfolg beim Einsatz von Stammzellen bei der Hauterkrankung Epidermolysis bullosa (Schmetterlingskrankheit). Verantwortlich ist dafür ein fehlerhaftes Protein namens Laminin-322. Aus Stammzellen eines Jungen wurde das defekte Gen entfernt und durch das richtige ersetzt. Dann wurde das neue Hautgewebe vermehrt und dem Jungen übertragen. Heute (2017) nach zwei Jahren kann der Junge wie ein gesundes Kind agieren. Auch reagiert seine Haut jetzt völlig normal. Im Februar 2017 erscheint in Nature 542 ein Artikel des Japaners Nakauchi, der davon berichtet, dass es mit Hilfe von iPS-Zellen.von Mäusen gelungen sei, einen Rattenembryo, dem zuvor die Bauchspeicheldrüse entfernt wurde, zur Bildung einer Mäusebauchspeicheldrüse zu veranlassen. Im Juli 2019 folgte der Bericht darüber, dass nunmehr in Mäuseembryonen, denen zuvor die Bauchspeicheldrüse entfernt wurde, iPS-Zellen des Menschen eingesetzt werden sollen. Dieses Forschungsvorhaben ist vom Japanischen Forschungsministerium genehmigt worden, allerdings nur für die Universität Tokio. Der deutsche Molekularbiologe Reich äußerte dazu große Bedenken, dass die Folgen nicht absehbar seien. |
1.7. Praeimplantationsdiagnostik (PID) Bei der
Praeimplantationsdiagnostik werden Eizellen in vitro befruchtet und die
ersten sich bildenden Zellen werden auf genetische Schäden untersucht. Die
Embryonen mit Schäden werden verworfen, die gesunden implantiert. Dieses
Verfahren ist in Deutschland verboten, nicht aber z. B. in England und den
USA. In den USA werden sogar Untersuchungen auf das Geschlecht zugelassen!
2. Biotechnologie mit Veränderung der Gene (Genetic-Engineering). Hier ist es notwendig -
zumindest in Kurzform - eine Übersicht über die Verschlüsselung und
Weitergabe der Erbanlagen zu geben. Alle Körperfunktionen werden
letztendlich über Proteine (Eiweiße) und Proteide (eiweißähnliche
Moleküle) gesteuert. Das bedeutet, dass in den Genen die Struktur der
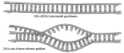
Proteine und Proteide verschlüsselt sein muss. Die Gene sind fadenförmige,
zu einer "Doppelschnecke" (Doppelhelix)
Die Reihenfolge der organischen Basen in
der DNS bestimmt die Reihenfolge der Aminosäuren in dem Protein,
2.0. Einschleusen von Genen in die Zelle. 2.0.1. Viraler Gentransfer Retroviren: Sie werden in das Empfängererbgut integriert, jedoch läßt sich der Einbauort nicht festlegen. So können sich die Spendergene in vorhandene Gene einlagern und diese somit schädigen. Mit Retroviren kann jedoch nur bei sich teilenden Zellen gearbeitet werden. Adenoviren: Sie bleiben frei in der Zelle. Mit ihnen kann man in sich teilenden Zellen aber auch alten Zellen arbeiten. 2.0.2. Nicht-viraler Gentransfer Mikroinjektion Ballistische Injektion Calcium-Phosphat-Methode Elektroporation Über Liposomen
2.1. Genchirurgie zur Heilung defekter Gene. Hierbei geht es darum, einzelne
Basen der DNA wieder zu reparieren, wenn falsche eingebaut worden sind. Eine Krankheit,
die dazu gehört, ist die so genannte Sichelzellenanämie, bei der sich die roten
Blutkörperchen sichelförmig verändern. Der Fehler liegt im Einbau der Base Thymin an
Stelle von Adenin, so dass das Basentriplett ...GTG... statt ..GAG... entsteht, was
wiederum bedeutet, dass statt der Aminosäure Glutaminsäure (Glu) die Aminosäure Valin
(Val) eingebaut wird (siehe Codesonne). Jetzt könnte also das richtige Gen an Stelle des
falschen (mutierten) eingebaut werden und alles wäre wieder in Ordnung. Dies müsste
allerdings in den Keimzellen geschehen, um die Krankheit endgültig aus dem Erbgeschehen
auszuschließen.
2.2. Genchirurgie durch Einbau fremder Gene. Hier werden fremde Gene (Transgene) in ein Lebewesen eingeschleust, um sie zu veranlassen, etwas zu tun, was die Empfänger normalerweise nicht können. Es entstehen so genannte "transgene" Lebewesen. Bei Pflanzen wurde dies erstmals 1980 durchgeführt. 2.2.1. So können z. B. Gene in
Pflanzen eingebracht werden, um sie resistent (widerstandsfähig) gegen Insektenfraß,
Bakterien- bzw. Pilzbefall zu machen oder z. B. gegen den Befall durch Nematoden zu
schützen, wodurch das Spritzen der Pflanzen mit entsprechenden Pestiziden, Fungiziden und
Insektiziden entfallen könnte. Sie können auch resistent gemacht werden gegen salzige
Böden, indem man aus Salz gewohnten Pflanzen die entsprechenden Gene gewinnt und sie
überträgt. 2.2.2. Es können menschliche
Gene in Bakterien eingeschleust werden, die diese veranlassen, menschliche Stoffe
herzustellen, so z. B. menschliches Insulin oder den Faktor VIII, der den Hämophilen
(Blutern) fehlt. Weitere von Bakterien produzierte Human-Proteine sind: Wachstumshormone,
Interferon (Virostatikum), Parathormon (reguliert den Calciumstoffwechsel), Somatostatin
(reguliert die Produktion von Wachstumshormonen), Relaxin (entspannt den Uterus),
c-Endorphin (stillt Schmerzen), Urokinase (löst Thromben), Superoxid-Dismutase (hemmt
Entzündungsprozesse), Hepatitis-Antigen (Vakzin gegen Hepatitis), Tumor-Nekrose-Faktor
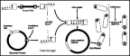
(inhibiert das Wachstum von Tumorzellen). Man baut nun ein Human-Gen in ein
Plasmid ein. Damit man dieses Plasmid später wieder findet und von anderen unterscheiden
kann, baut man auch ein Erkennungsmerkmal ein, in unserem Beispiel ist es ein Resistenzgen
gegen Antibiotika. Mit Hilfe von Restriktionsenzymen (Schneideenzyme, das erste wurde 1972
beschrieben) schneidet man das Plasmid an vorbestimmten Stellen auf, wobei so genannte
sticky (clipsy) ends ("klebrige Enden") frei werden und baut dann mit Hilfe des
Enzyms DNA-Ligase ("DNA-Klebstoff") das Human-Gen ein. Dann werden die so
manipulierten Plasmide vermehrt (dies ist im Prinzip eine Gen-Klonung) und in die
gewünschten Bakterienzellen eingeschleust. Um jetzt sicher zu gehen, dass anschließend
nur noch mit den transformierten Bakterien gearbeitet wird, werden die Zellen mit
Antibiotika behandelt. Nur die Bakterien überleben, die resistent sind. Und das sind
genau die, in denen die eingeschleusten Plasmide sind, denn denen wurde ja die Resistenz
gegen Antibiotika mit eingebaut. Diese Methode ist mit Recht in die Kritik geraten, weil
man hier unnötigerweise Resistenzgene gegen Antibiotika einsetzt. (siehe
auch unter 1.1.2.) 2.2.3. 1998 wurden von der
amerikanischen Firma "Genzyme" durch Klonen drei Ziegen gezeugt, die in ihrem
Erbgut das menschliche Gen für den Blutgerinnungsfaktor Antithrombin III (ATIII)
enthielten. Dieses ATIII konnte auch in der Milch nachgewiesen werden, so daß ATIII aus
der Milch gewonnen werden kann. Bisher konnte ATIII nur aus Spenderblut in geringsten
Mengen gewonnen werden. 2.2.4. Die oben erwähnten
Methoden werden auch angewandt, um tierische Organe für die Transplantation auf den
Menschen zu präparieren. Das Problem, das dabei auftaucht, ist die Abstoßung fremder
Organe. Der menschliche Körper erkennt das fremde Gewebe als nicht körpereigen und
trennt sich von ihm (Antigen-Antikörper-Reaktion). Nun kann man menschliche Gene in die
Tiere übertragen, die für Transplantationen vorgesehen sind. Diese Technik nennt man
Xenotransplantation (xenos = fremd). Überträgt man nun die manipulierten tierischen
Organe auf den Menschen, so werden sie nahezu wie eigenes (menschliches) Gewebe betrachtet
und die Abstoßungsreaktion fällt deutlich weniger heftig aus. 2.2.5. Eine weitere Methode geht einen anderen Weg. Man schwächt das Immunsystem eines Tieres (z. B. das einer Maus) und überträgt in dieses Tier beispielsweise menschlichen Knorpel. In der Maus wächst so eine menschliche Ohrmuschel. Hier werden keine Gene, sondern Zellen übertragen (siehe Abbildung rechts.) 2.2.6. Herstellung von Impfstoffen (Vakzine) mit Hilfe von ungefährlichen DNA-Abschnitten infektiöser Viren. 2.2.6.1. Es werden DNA-Abschnitte von Viren in Plasmide eingebaut und durch Vermehrung der Bakterien vervielfacht. Die so gewonnen DNA-Partikel ("nackte DNA") werden auf Goldkügelchen aufgebracht und mit einer speziellen Gen-Impfpistole unter die Haut gebracht. Der Körper reagiert mit Antikörperbildung. Erfolgreich war diese Methode gegen Hepatitis B an 12 Versuchspersonen im Jahr 1999, wie der Impfpistolen Hersteller PowderJect berichtete. 2.2.6.2. Auch hier werden DNA-Abschnitte der Viren gewonnen, aber diesmal in andere Lebewesen ("Live Vector") eingebaut, zum Beispiel in Tomaten und Spinat (gegen Tollwut), Kartoffeln (gegen Hepatitis B), Melonen (gegen Cholera) oder Langbohnen zum Schutz von Hunden gegen den Durchfall auslösenden Parovirus (CPV-2). Experimentiert wird hier sehr viel, so in Deutschland bei MediGene Ende 1999 mit dem Papillomavirus (HPV), der Gebärmutterhalskrebs auslöst. (Nobelpreis 2008) 2.2.6.3. Diese Methode wendet man auch an, um nach Operationen bösartiger Tumore die Abwehr der Patienten gegen Neu-(Wieder-)Infektion zu erhöhen, indem man genetisch veränderte Tumorzellen ("Pharmaccinen") injiziert. Ein fertiger Impfstoff gegen Darmkrebs (OncoVAX) liegt in den Niederlanden vor. Weitere Impfstoffe sind in der Vorbereitung. 2.2.7. Es gibt in der Natur auch Tiere, z. B. Insekten, die die Fähigkeit verloren haben, ihre in ihnen lebenden Krankheitserreger weiterzugeben. So gibt es Anopheles Mücken, die den Malariaerreger Plasmodium nicht weitergeben können. Diese Tiere werden "refraktär" genannt. Deren Gene wollte man bereits in den Sechzigerjahren durch Züchtung oder Übertragung (Transgene) weitergeben. Doch die Probleme waren zu groß.2.2.8. In der Universität Göttingen wurden 1999 Gene bei Mäusen entdeckt, die Inselstammzellen in der Bauchspeicheldrüse aktivieren können. So könnten diese Gene bei Menschen eingeschleust werden und die noch vorhandenen Stammzellen zur Insulinbildung veranlassen. Erfolg wird in etwa 7 Jahren erwartet (nach heutigem Wissensstand). 2.2.9. In den Vierzigerjahren entdeckte Barbara McClintock (Nobelpreis 1983) "springende Gene" im Mais. In den Siebzigerjahren wurden dann die "springenden Gene" (genauer: Transposons) bei Drosophila melanogaster entdeckt. Sie führten zu bestimmten Missbildungen und Chromosomenbrüchen, wenn Männchen aus bestimmten Populationen mit Weibchen einer anderen Population gekreuzt wurden. Man entdeckte dann den so genannten "P-Faktor" (Paternal-Faktor), der sich als Transposon erwies. Damit war eine Technik der Genübertragung neben der über Viren entdeckt worden. 2.2.10. Bakterien, speziell E. coli, werden genmanipuliert und stellen aus Maisstärke Moleküle mit dem Kürzel PDO her, die zu komplexen Kettenmolekülen mit dem Namen SORONA, einem Kunststoff , verknüpft werden (Firma DuPont 2006). Die amerikanische Firma METABOLIX (2006) erzeugt auf ähnliche Weise voll biologisch einen Kunststoff namens PHA. Die englische Firma ICI hatte in den achtziger Jahren schon einmal mit ihrem Kunststoff BIOPOL einen Versuch gestartet, war aber nicht erfolgreich. Da hier Naturprodukte, z. Stärke, eingesetzt werden, tritt das Problem der nicht beliebig verfügbaren Ausgangssubstanz auf, bzw. durch Kauf auf dem Markt werden deren Preise in die Höhe getrieben. Zudem steht nicht genügend Ackerfläche zur Verfügung. 2.2.11. Japanische Wissenschaftler haben 2007 in Reis ein Gen eingebaut, das Cholera-Toxine herstellt. Eine Reismahlzeit reiche dabei aus, um eine Infektion zu verhindern Dies hätten jedenfalls die Versuche an Tieren gezeigt. Sozusagen Impfung per Nahrungsaufnahme. 2.2.12. Japanische Wissenschaftler um Shigeto Yoshida von der Jichy Medical University in Tokio haben ein Gen, dass einen Impfstoff gegen Leishmaniose produziert, in ein Mückengenom eingebaut. Diese transgenen Mücken sind somit quasi lebende Impfen. Nachzulesen im Fachmagazin "Insect Molecular Biology" vom Frühjahr 2010. 2.3. Umbau, Neubau, Abschalten und Ausbau von Genen 2.3.3. In der Princeton University/USA wurde 1999 ein Gen bei Mäusen verändert, dass die Bildung des NMDA-Rezeptors erhöht. Das führt dazu, dass dieses Protein die Verknüpfung der Nervenzellen erhöhte und somit die Gedächtnisleistungen der behandelten Mäuse deutlich verbesserte (vier- bis fünfmal). Hier könnte ein Schlüssel für die Behandlung von Demenz-Krankheiten liegen. 2.3.4. Um den
Mangel an transplantationsfähigen Organen zu umgehen, bieten sich
entsprechende tierische Organe von z. B.
2.3.5. Die
Zeitschrift "Science" meldet Anfang 2008, dass Forscher um den
amerikanischen Genetiker Craig Venter ein komplettes Bakteriengenom aus
Einzelbausteinen hergestellt haben. Dieses künstliche Genom soll nun
Schritt für Schritt wieder um einzelne Gene abgebaut werden, um
festzustellen, welche Gene für das Bakterium lebensnotwendig sind und
welche nicht.
2.3.6. Indische Forscher haben im Januar 2010 laut "Proceedings" der US-Akademie der Wissenschaften bei Tomaten zwei Enzyme unterdrückt, die für vorzeitiges Reifen verantwortlich sind. Sie schalteten entweder das Enzym a-Mannosidase oder ß-D-N-Acethylhexosaminidase ab. Diese Enzyme kommen auch in anderen Früchten, z.B. Bananen und Mangos, vor. In Indien gehen 35 40% der Ernte durch zu schnelles Weichwerden verloren.
Das Crispr/Cas9-System, das seit 2012 die Gentechnik von Grund auf verändert, nimmt Anleihen bei einem ausgeklügelten bakteriellen Immunsystem, das vor Viren schützt. Es basiert auf einer adaptiven Immunabwehr, die sich DNA-Sequenzen der Erreger "merkt" und bei einer erneuten Infektion deren DNA zerschneidet. Diese Kombination aus Erkennen und Schneiden macht man sich beim Gene Editing zu Nutze. Bei der einfachsten Variante injiziert man RNA in die Zelle, die ein Protein namens Cas9 und eine beliebige Erkennungssequenz kodiert. Die Zelle stellt anhand der RNA das Protein her, dieses findet die beigefügte Erkennungs-RNA und geht an die Arbeit: Cas9 schneidet doppelsträngige DNA – und zwar genau an der Stelle, die ihm das assoziierte RNA-Stück vorgibt. Da man RNA mit einer beliebigen Sequenz künstlich herstellen kann, schneidet eine solche Kombination jedes beliebige Genom an jeder beliebigen Stelle, zumindest theoretisch. Bereits seit den 1980er Jahren kennt man die so genannten CRISPR-Sequenzen im Erbgut: Die Abkürzung steht für "clustered regularly interspaced short palindromic repeats", also kurze palindromische Wiederholungssequenzen, die durch andere Erbgutstücke getrennt sind und im Genom an bestimmten Stellen gehäuft auftreten. Die Erbgutstücke zwischen den wiederholten Sequenzen, stellte sich dann heraus, stammen oft von Viren – ein Indiz, dass die CRISPR Teil eines antiviralen Systems sein könnten. In der Nähe der CRISPR fand man später bei allen Bakterien mit diesem System die CRISPR-assoziierten Gene, Cas genannt. Sie sind das entscheidende Element des antiviralen Systems. Das CRISPR-System "erntet" virale DNA und integriert Stücke von ihr zwischen den Wiederholungssequenzen ins bakterielle Erbgut. Dadurch produziert die Zelle RNA-Gegenstücke zur Virus-DNA, die sich mit den Cas-Proteinen zusammenfindet. Versucht ein Virus mit dieser DNA die Zelle noch einmal zu infizieren, "erkennt" die RNA das Viren-Genom: Die Cas-Proteine zerschneiden dann das virale Erbgut, so dass es keinen Schaden mehr anrichtet. Ursprung des Gene Editing ist die Erkenntnis, dass die Cas-Proteine jede beliebige DNA zerschneiden, sofern man ihnen die passende Erkennungs-RNA mitgibt. Mehr macht CRISPR/Cas9 auch nicht: Nach dem Schnitt verlässt man sich auf die natürlichen Reparaturmechanismen der Zelle, die nun von selbst zum Tragen kommen. Sind in diesem Augenblick nur die beiden getrennten Teile des Erbguts vorhanden, greift ein zellulärer Reparaturmechanismus, der sie wieder zusammenfügt – der aber ist oft unpräzise und produziert zufällig so genannte Indels, kleine DNA-Stücke, die an der Schnittstelle eingefügt oder ausgeschnitten werden und Gene unter Umständen unbrauchbar machen. Wenn in der Zelle aber ungebundene DNA mit losen Enden herumschwirrt, baut ein anderes, genaueres System (HDR, homology-directed repair) sie nahtlos an der In der biotechnischen Forschung hat CRISPR/Cas9 inzwischen seinen festen Platz als Gentechnik-Werkzeug gefunden, auch jenseits seiner ursprünglichen Form. Unter anderem regulieren seine Abkömmlinge im Labor gezielt Genaktivität. Dazu verwendet man ein inaktiviertes Cas9, das sich lediglich fest an spezifische DNA-Stücke anheftet. Bindet so ein Protein an eine Aktivator-Domäne, erhöht sie zum Beispiel die Aktivität des zugehörigen Gens. Wenn es dagegen die Gensequenz selbst blockiert, kann der entsprechende Sektor des Erbguts schlicht nicht mehr in RNA übersetzt werden. Mit Hilfe verschiedener, an inaktive Cas9-Systeme gebundener Proteine kann man inzwischen auch epigenetische Effekte erforschen, zum Beispiel indem man durch Fluoreszenz die räumliche Lage bestimmter Sequenzen markiert. Durch gebundene Enzyme, die Methyl- oder Azylgruppen abspalten oder anfügen, können solche CRISPR/Cas9-Systeme auch die Epigenetik in Zellen gezielt verändern. Vor allem aber produziert man mit CRISPR/Cas9 heute sehr effektiv genetisch veränderte Organismen: Lebewesen, bei denen dank einer Mutation ein bestimmtes Gen verändert, eingefügt oder unbrauchbar gemacht wird. Solche Verfahren sind weit älter als CRISPR. So erhielten bereits 2007 die Erfinder des so genannten Gen-Knockouts den Nobelpreis für Physiologie oder Medizin. Doch CRISPR/Cas9 ist schneller, billiger und auch vielseitiger als die älteren Verfahren. Im Labor kann man auch eines der zentralen Probleme von CRISPR umgehen: die Größe der nötigen RNA. Inzwischen gibt es zum Beispiel diverse Mäuserassen, die das Cas9-Protein im eigenen Erbgut tragen – sobald ein bestimmtes molekulares Signal samt passender Erkennungs-RNA in die Zelle gelangt, steht das Molekül Gewehr bei Fuß, um das Erbgut zu verändern. Die ersten veränderten Organismen für praktische Anwendungen jenseits der Grundlagenforschung sind ebenfalls bereits in Arbeit. Auf diese Weise wird man, wenn es nach den Plänen der beteiligten Forscherinnen und Forscher geht, in Zukunft bessere Tiermodelle für menschliche Krankheiten herstellen, ebenso wie Nutztiere und -pflanzen mit bestimmten Eigenschaften, zum Beispiel Anopheles-Mücken, die gegen Malaria resistent sind. Ein interessantes Beispiel ist eine Genombereinigung einer Arbeitsgruppe, die das Erbgut eines Schweins von den potenziell gefährlichen Retroviren befreite – eine wichtige Voraussetzung für den Plan, in Tieren menschliche Spenderorgane zu züchten. Außerdem ist aus CRISPR/Cas9 der so genannte Gene Drive hervorgegangen – ein Mechanismus, mit dem sich bestimmte künstliche Eigenschaften schnell in Wildtierpopulationen verbreiten. Interessant ist das zum Beispiel für die Bekämpfung von Moskitos in Regionen, in denen sie gefährliche Krankheiten übertragen. Ebenfalls im Blickfeld der medizinischen Forschung sind CRISPR/Cas9-basierte Instrumente gegen Viren und Bakterien – mit Hilfe des Gene Editings soll die DNA dieser Erreger gezielt an für sie spezifischen Orten geschnitten werden. Allerdings ist noch völlig unklar, wie man die nötige RNA bei einer realen Erkrankung an den gewünschten Ort bringt. © Spektrum.de Diese neue Gentechnik beunruhigt viele Menschen, weckt aber auch neue Hoffnung bei der Bekämpfung von Erkrankungen. So zum Beispiel bei der Sichelzellenanämie oder der Borreliose. Benutzt wird sie in den USA bei der Getreidezüchtung. Da dabei in der Regel keine Gene importiert werden, sind diese Manipulationen nicht meldepflichtig. Bedenken äußert auch der Deutsche Ethikrat. In einer Plastikschale in seinem Labor hatte He
Jiakui im November 2018 bekannt gegeben, dass er einen gentechnischen
Eingriff am Erbgut von Zwillingen vorgenommen hat, als diese noch
Embryonen waren. Mit der noch jungen gentechnischen Methode names
Crispr/Cas9 sollten die Kinder demnach resistent gegen HIV gemacht
werden. Eine unabhängige Bestätigung für die Behauptung gibt es bislang
nicht. Bekannt sind allein die Aussagen von He Jiankui. Die Identität
der Kinder will der Wissenschaftler geheim halten. Seine Mitteilung rief viel Protest hervor und Wissenschaftler warnen vor solchen Versuchen an Menschen, da deren Auswirkung noch völlig unbekannt sei. Laut dpa vom November 2019 hat am Universitätsklinikum Regensburg eine Gen-Therapie gegen die angeborene Bluterkrankheit Beta-Thalassämie erste Erfoge erzielt. Bei der Therapie der Klinik in Regensburg wurden der 20jährigen Patientin blutbildende Stammzellen entnommen und mit einem Crispr/Cas9-Verfahren bearbeitet. Die so entstandenen Stammzellen begannen funktionstüchtige Blutzellen zu bilden. Es wurden hierbei keine Gendefekte korrigiert, sondern ein alternatives Gen zur Blutbildung aktiviert, das von Geburt an da ist. Die Patientin weist seit neun Monaten normale Blutwerte auf 2.5. Genkartierung.Es ist schon länger möglich, defekte menschliche Gene mit so genannten Gensonden nachzuweisen. 1993 hat man nun eine wesentlich elegantere Methode entwickelt, die zudem schneller als die alte ist, den so genannten gläsernen Gen-Chip.  Er
basiert auf dem altbekannten molekularbiologischen Prinzip der Hybridisierung. (siehe
Abbildung rechts). Er
basiert auf dem altbekannten molekularbiologischen Prinzip der Hybridisierung. (siehe
Abbildung rechts).
Der Chip ist 1,28 cm˛ groß und hat genau 65.536 Felder. Auf jedem Feld steht eine Kette von acht DNS-Bausteinen, denn so viele Möglichkeiten der Kombination von vier Basen gibt es. Die zu untersuchenden DNS-Abschnitte passen also immer nur auf eines dieser Felder. Nur wenn der komplementäre Abschnitt auf dem Chip aufsitzt, leuchtet dieser Abschnitt auf Grund einer speziellen Behandlung auf und wird vom Computer erfasst, der natürlich genau weiß, welche Basenkombination wo auf dem Chip sitzt. Es gibt seit 1996 einen weiteren Chip, der 64.000 Felder mit Ketten von 20 DNS-Bausteinen aufweist, der noch leistungsfähiger ist. dpa meldete am 5. April 2000, dass es der amerikanischen Firma "Celera Genomics Corp." in Rockville (Maryland) gelungen sei, 99% des Genoms aufzuschlüsseln, schneller also als erwartet und schneller als durch das Projekt HUGO. (HUGO = Human Genome Organization: Ein Projekt zur Erforschung des menschlichen Erbgutes, das 1986 von dem Amerikaner Renato Dulbecco initiiert wurde und an dem sich weltweit (circa 50 Länder) viele Institute beteiligen.). Im Mai 1998 wurde bereits bekannt, dass der amerikanische Genetiker Craig Venter, Präsident von Celera, mit Hilfe von 200 Sequenzier-Robotern vom Typ ABI PRISM der Firma Perkin-Elmer in drei Jahren die Aufgabe erledigt haben will (er war sogar schneller, wie gemeldet wurde. s.o.). Inzwischen wird jedoch berechtigterweise bezweifelt, ob Celera wirklich so weit ist. Das Projekt HUGO, das bis jetzt etwa sechs Milliarden DM verbraucht hat, könnte sich dann mit seinen Geldern um die Aufschlüsselung der Funktion der Gene kümmern. HUGO hat im April 2000 zwar nur etwa 90% des Genoms aufgeschlüsselt, doch sind die Gene weitgehend geordnet, was Celera noch machen muss. Am 26. Juni 2000 nun erklärten Celera und HUGO in einer Pressekonferenz in Anwesenheit des US-Präsidenten Bill Clinton und des englischen Premierministers Tony Blair, daß beide Organisationen zusammenarbeiten wollen und z. Z. 97% der Nucleotide entschlüsselt hätten. Damit würde die Diagnose von Gendefekten an Embryonen im 4 – 8 Zellstadium sehr schnell erfolgen können und damit vielleicht auch bald deren Beseitigung. Damit wäre auch das Kurieren an Symptomen beendet und die eigentliche Behebung (Beseitigung) von Krankheiten könnte beginnen. Dies ist jedoch noch ein sehr weiter Weg, wie auch der deutsch-amerikanische Nobelpreisträger Prof. Dr. Günter Blobel feststellte. Es gibt beispielsweise über 700 einzelne Gendefekte des CF-Gens, das für die erbliche Stoffwechselkrankheit Muskoviszidose verantwortlich ist. Das CF-Gen reguliert den Transport von Wasser und Salzen durch die Zellmembranen. Mitte 1997 waren etwa 6.500 der vermuteten etwa 30.000 (ohne deren Steuerungsgene!) menschlichen Gene vollständig dechiffriert und auf einem Chip untergebracht. Im Dezember 1999 wurde bekannt, dass die Gene (oder nur die Nucleotide?) des Chromosoms 22 vollständig aufgelistet werden konnten. Am 9. Mai 2000 wurde die Entschlüsselung des Chromosoms 21 bekannt gegeben. Im Mai 2006 wurde schließlich die Entschlüsselung des Chromosoms 1, und damit die des letzten Chromosoms, bekannt gegeben (Nature). Die Genauigkeit der Sequenz wird mit 99,99 % angegeben. Im Frühjahr 2000 wurde das gesamte Genom von Drosohila melanogaster, dem "Haustier" der klassischen Genetiker entschlüsselt. In der Krebsmedizin wird der Chip der Firma Affymetrix zum Nachweis von Defekten bei dem Tumorsuppressor-Gen p53 eingesetzt, um auf diese Weise u. a. gesundes von krankem Gewebe eindeutig unterscheiden zu können. Der Chip arbeitet so empfindlich, dass er noch eine onkogene Zelle unter 10.000 gesunden herausfindet. Ab Mai 1998 wurde an der Entschlüsselung der Funktion von p53 gearbeitet und laufend kommen neue Teilerkenntnisse hinzu. Beim Menschen unterscheidet sich nur 0,1 % der DNA voneinander, oder anders ausgedrückt: 99,9 % der DNA der Menschen ist gleich. (Zur Information: Maus und Mensch haben 98% der Gene gemeinsam!) Mann hofft, in drei Jahren das gesamte menschliche Genom erfasst zu haben (siehe auch weiter oben). Dabei sollen vor allem die etwa 150.000 individuellen Merkmale des Menschen herausgestellt werden durch Erstellung einer SNP-Karte (single nucleotide polymorphism, [snip gesprochen]). Anhand solcher SNP-Biochips lassen sich dann möglicherweise Krankheiten früh erkennen. Ihre Funktion zu begreifen und sie letztendlich zu beeinflussen dürfte aber wesentlich länger dauern. Etwa 3000 - 4000 Krankheiten beruhen auf Erbfehlern. Brauchte vor 10 Jahren ein Doktorand noch 3 Jahre für die Sequenzierung eines Gens, so ist man 1999 1000 Mal so schnell. Die Genetische Information des Menschen besteht aus etwa 3,5 Milliarden Buchstaben (Nucleotiden) und ergibt etwa ein Gigabyte an Daten. Im Frühjahr 2009 veröffentlichten Forscher des Baylor College of Medcine in Texas das Genom der Kuh. Es besitzt etwa 22.000 Gene, von denen über 14.000 schon von anderen Säugern bekannt sind. Die Forscher um Richard Gibbs erklärten, dass etwa 80% der Gene mit dem Menschen übereinstimmen und dass die Kuh mit dem Menschen näher verwandt sei als mit Mäusen und Ratten. 2.5.1. Der kanadische Genetiker Paul Hebert von der University of Guelph hat ein Gen entdeckt, das von Tierart zu Tierart variiert. Damit könnte man schnell unbekannte Tiere aufgrund deren Basenfolgen erkennen. Das Zuordnen müßte dann noch durch Taxonomen erfolgen. 2.6. GentherapieEnde 1999 gelang es Ärzten in
Paris Kinder mit SCDI-Syndrom erfolgreich zu behandeln. Sie entnahmen den Kindern
Knochenmark und injizierten es mit Viren, die das gesunde Gen enthielten. Anschließend
wurde das so behandelte Knochenmark zurückinjiziert. Einige Wochen später wurden bei den
Kindern normal hohe Anzahlen an T-Lymphozyten festgestellt. Im Januar 2016 wird gemeldet, dass in Großbritannien die HFA (Human Fertilisation and Embryology Authority) dem Londoner Francis Crick Instutute die Genehmigung erteilt hat, an menschlichen Embryonen bis zum Alter von 7 Tagen gentechnische Versuche durchzuführen. Dies soll der Erforschung der Vorgänge in den ersten sieben Tagen nach der Befruchtung einer Eizelle dienen, um die Erfolgsrate bei der künstlichen Befruchtung zu erhöhen. Es geht dabei speziell um das Verfahren CRISPR/Ca9. Das Verfahren wird schon länger von der Gruppe um Kathy Niakan angewendet. 2.7. DNA-Nanoroboter Laut der Zeitschrift "Science" gelang es 2012 Forschern der Harvard-Universität Boston um Shawn Douglas einen Nanoroboter herzustellen, der DNA gezielt an bestimmte Ziele eines Organismus transportieren kann. Er ist bisher nur an Zellkulturen erprobt, so dass noch unklar ist, ob er auch beim Menschen funktioniert. Der Roboter ist ein sechseckiger Käfig mit einer Höhe von 45 nm und 35 nm Dicke, versehen mit einem Riegel, mit dem er an bestimmten Zellen andocken kann, um so z.B.eine DNA einzuschleuse, die das Selbstmordprogramm einer Zelle (Krebszelle) aktivieren kann. 2.8. Impfstoffe durch Gentechnik 2012 wurde bekannt, dass bei der Firma Novartis
Vaccines in Sienna Rino Rappuoli an einem Impfstoff gegen
Meningokokken B arbeitet und erste Erfolge erzielt hat. Durch
Aufschlüsselung des Genoms werden die Stellen am Genom gesucht, an denen
durch gezielte Eiweißbildung gegen die Meningokokken ein Impfstoff
produziert wird. Diese Methode verspricht auch schnell Impfstoffe finden
zu können, die sich gegen resistente Staphylococcus aureus-Stämme richtet.
Auch könnte schneller auf neue Grippeviren reagiert werden. Hier werden
sozusagen neue Impfstoffe designt. UCART19, an
allogeneic “off-the-shelf” adoptive T-cell immunotherapy against CD19+
B-cell leukemias. Das ist eine Nachricht vom Dezember 2015 aus dem London
Great Ormond Street Hospital, wo ein ein Baby von einer akuten lymphoblastischen
Leukämie geheilt wurde. Dieses Ergebnis ist ein großer Erfolg für das Kind
und ein Hoffnungsschimmer für weitere Erkrankte. 2.9. Gensteuerung (Epigenetik) (Siehe auch 6) Darauf soll nur kurz eingegangen werden. Die Steuerung erfolgt z. B. über anabolische und katabolische Operons, bei deren Kenntnis man gezielt in die Proteinsynthese eingreifen und somit die Tätigkeit von Genen beeinflussen kann. Eine andere Art der Steuerung von Genen erfolgt über Methylierung von DNA-Abschnitten. Methylgruppen führen zum Abschalten von Genen, die dann von Histonen dicht verpackt werden, was auch vererbt werden kann. Im Dezember 2006 hat Prof. Albert Jetsch von der IUB in Bremen dazu gezielte Versuche gemacht und Gene abgeschaltet. Es wurden auch RNA-Abschnitte gefunden, die die Translation beeinflussen und deren Bau vererbt wird. Hier ist noch alles im Fluss und dürfte recht interessant werden. 3. Genetisch veränderte Bakterien zur Krebsbekämpfung. Zur Zeit (2015) wird in mehreren Ländern an dieser Fähigkeit der Krebsbekämpfung gearbeitet. In Deutschland sind es Forscher des HZI in Braunschweig (Siegfried Weiß, Sara Bartels), die mit genetisch abgeschwächten Salmonellen, die noch zusätzliche Gene eingebaut bekommen, arbeiten. In den USA sind es Forscher um Daniel Portnoy von der Universität von Kalifornien, die mit Listerien arbeiten. So konnten sogar Patienten mit Bauchspeicheldrüsenkrebs über Jahre behandelt werden. Ferner Tom Dubensky von der Firma Aduro Bio Tech. Die Listerien können auch als Vehikel zum Transport radioaktiven Materials in die Krebszellen genutzt werden. An der John Hopkins Universität in Baltimore sind es Shibin Zhou und Mitarbeiter, die mit Clostridium novyi arbeiten. Nähere Einzelheiten findet man auf den Webseiten der jeweiligen Institute und auch im FOKUS 16/2015. 4. DNA-Verwertung in der Elektronik.
5. Verwendung ganzer Zellen (Zellchip).  In der Universität von
Kalifornien wurden Zellen in computergesteuerte Schaltkreise eingebaut (siehe
Abbildung links).
Deren Zellmembranen werden bei Anlegung geringer Spannungen durchlässig, was das
Einschleusen von Substanzen und genetischer Informationen erleichtert. Dies hat mit
Genmanipulation nicht direkt zu tun, zeigt aber den Weg, den die Biologie geht. In der Universität von
Kalifornien wurden Zellen in computergesteuerte Schaltkreise eingebaut (siehe
Abbildung links).
Deren Zellmembranen werden bei Anlegung geringer Spannungen durchlässig, was das
Einschleusen von Substanzen und genetischer Informationen erleichtert. Dies hat mit
Genmanipulation nicht direkt zu tun, zeigt aber den Weg, den die Biologie geht.
Die Epigenetik befasst sich mit der Expression der
Genome (man spricht daher auch von Epigenomen). Nicht allein die Abfolge
der Nukleotide in den DNA-Strängen entscheidet über die Gestalt der Zelle,
sondern vielmehr angehängte Methylgruppen spielen eine große Rolle.
Sie bestimmen letztendlich ob Sequenzen der DNA abgelesen oder in welcher
Richtung sie abgelesen werden. Forscher um Ryan Lister des Salk-Institutes in La Jolla (Kalifornien)
haben im Hebst 2009 ein Epigenom (auch Methylom genannt) des Menschen
aufgeschlüsselt.
Eine Auseinandersetzung mit diesen teilweise sehr problematischen Folgen muss stattfinden, denn der Fortschritt der Wissenschaft - wie immer man diesen auch betrachtet - ist nicht aufzuhalten. Die Neugier der Forscher ist weder durch eindeutige, schon gar nicht durch unklare Regeln zu bremsen, wenn überhaupt. Auch muss diskutiert werden, ob eine Beschränkung der Forschung durch Verbote zulässig oder sinnvoll ist. 1999 arbeiteten in Deutschland 50.000 Menschen in der Gentechnikbranche. Für 2002 werden 150.000 Beschäftigte erwartet. 1996 gab es 75 Betriebe, Ende 1998 bereits über 400. Zum Vergleich für Europa: Freilandversuche fanden statt in Deutschland von 1994 bis 1997 77, in Großbritannien 149, in Frankreich 337, in den Niederlanden 90, in Belgien 91, in Spanien 85, in Italien 167. Andere europäische Länder lagen (teilweise deutlich - Irland 2) darunter. Für das Jahr 2000 rechnete man mit etwa 220 Produkten gegen Alzheimer, Parkinson, Krebs und weitere Krankheiten. Dies belebt die Wirtschaft und schafft viele neue Arbeitsplätze. Die hier genannten Zahlen sind offensichtlich nur Schätzungen, die teilweise zu hoch gegriffen sind. Eine Studie der Universität Oldenburg vom Frühjahr 2006 zeigt da andere Zahlenwerte auf. So nennt sie etwa 550 Firmen, die sich mit Gentechnologie befassen und die rund 12.000 Beschäftigte aufweisen. Doch auch diese Zahlen sind nur Schätzungen, da die von der Universität angeschriebenen Firmen sich sehr bedeckt gehalten haben. So findet man unter http://www.dbresearch.com Für das Jahr 2000 etwa 600.000 (weltweit?) Beschäftigte in der Biotechnologie, in 2005 schon 1.000.000. Für Deutschland werden 2004 15.400 Arbeitsplätze angegeben, allerdings nur für Kleinunternehmen. Auf der Seite von NRW werden 2007 für 1997(!) 1.800 Arbeitsplätze in der Biotechnologie angegeben und zusätzlich 2.300 Arbeitsplätze bei deren Zulieferer. Man hält sich also äußerst bedeckt, besonders bei den Großunternehmen. Ein Ergebnis der Genkartierung sind die "genetischen Fingerprints". Sie dienen der Überführung von Verbrechern, aber auch der Erkennung von Verwandtschaften längs verstorbener Menschen, indem deren Knochen-DNA (hält sich am besten) untersucht wird. In den USA werden von allen Verurteilten genetische Fingerprints genommen, in England seit 1995 von allen Verurteilten und Verdächtigen, in der BRD erst nur bei schweren Verbrechen, seit 1998 von allen dann Verurteilten und seit 1999 auch von bereits Verurteilten. Bei der Aufklärung von Verbrechen ist es auch möglich, die ethnische Herkunft des Materials zu bestimmen, was den Kreis der Verdächtigen sehr eingrenzen würde. Das ist in Deutschland jedoch verboten, nicht so in z. B. England und den Niederlanden. Die Versicherungsbranche verlangt schon vielfach den Nachweis, dass Gendefekte durch DNA-Analyse aufgezeigt werden und die Prämie dann entsprechend erhöht wird. Ist der Gendefekt nicht vererbt, entfällt sie. Die zu beantwortende Frage lautet: "Muss sich die Forschung nach der Ethik richten oder richtet sich die Ethik nach dem jeweiligen Stand der Forschung?" Eine weitere hochbrisante Frage ist dabei natürlich: "Wer bestimmt eigentlich, was Ethik ist?" O, Wonder! How many goodly creatures are there here! How beauteous mankind is! O brave new world, that has such people in 't! (Shakespeare.)
|